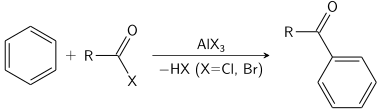親電芳香族取代是有機(jī)反應(yīng),其中與芳族體系(通常為氫)連接的原子被親電試劑取代。一些最重要的親電芳香取代是芳族硝化,芳族鹵化,芳族磺化和酰化和烷基化Friedel-Crafts反應(yīng)。
說(shuō)明性反應(yīng)
該反應(yīng)最廣泛實(shí)踐的例子是苯的乙基化。
1999年生產(chǎn)了大約24,700,000噸。[2](脫氫和聚合后,生產(chǎn)出商品塑料聚苯乙烯。)在這個(gè)過(guò)程中,固體酸被用作催化劑以產(chǎn)生初始碳陽(yáng)離子。苯的許多其他親電反應(yīng)被進(jìn)行,盡管規(guī)模小得多,它們是關(guān)鍵中間體的有價(jià)值途徑。苯的硝化是通過(guò)硝鎓離子作為親電子試劑的作用實(shí)現(xiàn)的。所述磺化用發(fā)煙硫酸使苯磺酸。與溴,氯的芳香鹵化或碘或相應(yīng)的芳基鹵化物。該反應(yīng)通常由相應(yīng)的三鹵化鐵或三鹵化鋁催化。
該Friedel-Crafts反應(yīng)可以作為進(jìn)行酰化或作為烷基化。通常使用三氯化鋁,但幾乎可以使用任何強(qiáng)的路易斯酸。對(duì)于酰化反應(yīng),需要化學(xué)計(jì)算量的三氯化鋁。
反應(yīng)機(jī)制
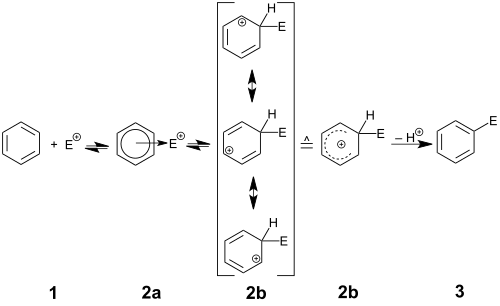
反應(yīng)機(jī)理,表示為S?E?Ar,以芳環(huán)攻擊親電試劑A?+開(kāi)始。該步驟導(dǎo)致形成帶正電和離域的環(huán)己二烯基陽(yáng)離子,也稱為鎓離子,Wheland中間體或σ絡(luò)合物。已經(jīng)表征了該碳陽(yáng)離子的許多實(shí)例,但是在正常操作條件下,這些高酸性物質(zhì)將附著于sp?3碳的質(zhì)子供給溶劑(或任何其他弱堿)以重新建立芳香性。最終結(jié)果是在芳環(huán)中用A取代H.?偶爾,H?+旁邊的其他電子氧化物將離去重新建立芳香;?這些物質(zhì)包括甲硅烷基(SiR?3),羧基(CO?2?H),碘基和叔烷基如叔丁基。這些類型的取代基,以留下的容量有時(shí)利用合成,特別是通過(guò)另一種官能團(tuán)(取代甲硅烷基的情況下本位取代)。然而,像I?+這樣的群體的喪失往往是不希望的副反應(yīng)。
取代基的影響
兩個(gè)區(qū)域選擇性?-the不同的可能的芳烴取代模式?-和速度的電芳族取代的由已經(jīng)連接到苯環(huán)上的取代基的影響。在區(qū)域選擇性方面,一些群體促進(jìn)了鄰位或?qū)ξ坏娜〈渌后w則傾向于在元位置取代。這些組分別稱為正交導(dǎo)向或元導(dǎo)向。此外,一些組將增加反應(yīng)速率(激活),而其他組將降低速率(停用)。雖然區(qū)域選擇性的模式可以解釋共振結(jié)構(gòu),對(duì)動(dòng)力學(xué)的影響可以通過(guò)共振結(jié)構(gòu)和誘導(dǎo)效應(yīng)來(lái)解釋。
反應(yīng)速度
關(guān)于親電取代,取代基通常可分為兩類:對(duì)芳環(huán)的活化和失活。?活化取代基或活化基團(tuán)通過(guò)感應(yīng)效應(yīng)或共振效應(yīng)將電子給予環(huán)系統(tǒng)來(lái)穩(wěn)定在取代期間形成的陽(yáng)離子中間體。活化芳環(huán)的實(shí)例是甲苯,苯胺和苯酚。
通過(guò)取代基遞送到環(huán)中的額外電子密度不是均勻地分布在整個(gè)環(huán)上,而是集中在原子2,4和6上,因此活化取代基也是鄰位/對(duì)位指導(dǎo)(見(jiàn)下文)。
另一方面,使取代基失活使中間陽(yáng)離子不穩(wěn)定,從而通過(guò)誘導(dǎo)或共振效應(yīng)降低反應(yīng)速率。它們是通過(guò)從芳環(huán)中提取電子密度來(lái)實(shí)現(xiàn)的。芳族體系的失活意味著通常需要更苛刻的條件來(lái)促使反應(yīng)完成。這方面的一個(gè)例子是在三硝基甲苯的生產(chǎn)過(guò)程中甲苯的硝化(TNT)。在活化的甲苯環(huán)上進(jìn)行的第一次硝化可以在室溫下進(jìn)行,并且使用稀酸,第二次硝化,在去活的硝基甲苯環(huán)上,已經(jīng)需要長(zhǎng)時(shí)間加熱和更濃的酸,第三次,非常強(qiáng)烈地失活二硝基甲苯,必須在沸騰濃硫酸中進(jìn)行。通過(guò)共振吸電的基團(tuán)降低電子密度,特別是在位置2,4和6處,使位置3和5作為具有相對(duì)較高反應(yīng)性的那些,因此這些類型的基團(tuán)是間位導(dǎo)向劑(參見(jiàn)下文)。鹵素是帶負(fù)電的,因此它們通過(guò)誘導(dǎo)失活,但它們只有一對(duì),因此它們是共振供體,因此是鄰位/對(duì)位指導(dǎo)。
具有未共享電子對(duì)的基團(tuán),例如苯胺的氨基,通過(guò)共振強(qiáng)烈活化和鄰位/對(duì)位取向。這些激活基團(tuán)將那些未共享的電子捐贈(zèng)給pi系統(tǒng),在鄰位和對(duì)位產(chǎn)生負(fù)電荷。因此,這些位置對(duì)于缺電子的親電試劑最具反應(yīng)性。最高的電子密度位于鄰位和對(duì)位,[?需要澄清?]盡管這種增加的反應(yīng)性可能被空間位阻所抵消取代基和親電試劑之間。因此,親電子芳族取代的最終結(jié)果可能難以預(yù)測(cè),并且通常僅通過(guò)進(jìn)行反應(yīng)并確定鄰位與對(duì)位取代的比率來(lái)確定。
除了原環(huán)的親核性質(zhì)增加外,當(dāng)親電試劑攻擊苯胺的鄰位和對(duì)位時(shí),氮原子可以向pi系統(tǒng)提供電子密度(形成亞胺離子),產(chǎn)生四種共振結(jié)構(gòu)(相對(duì)于三個(gè)在基本反應(yīng)中)。這顯著提高了陽(yáng)離子中間體的穩(wěn)定性。
當(dāng)親電試劑攻擊元位時(shí),氮原子不能向pi系統(tǒng)提供電子密度,僅給出三個(gè)共振貢獻(xiàn)者。這種推理與間位取代產(chǎn)物的低產(chǎn)率一致。
其他取代基,例如烷基和芳基?取代基,也可以向π系統(tǒng)提供電子密度;?然而,由于它們?nèi)鄙倏捎玫姆枪蚕黼娮訉?duì),因此它們的能力相當(dāng)有限。因此,它們僅微弱地激活環(huán)并且不會(huì)強(qiáng)烈地不利于元位置。
定向鄰位金屬化是一種特殊類型的具有特殊鄰位導(dǎo)向的EAS?。
具有比碳更具電負(fù)性的原子的非鹵素基團(tuán),例如羧酸基團(tuán)(-CO?2?H),從π系統(tǒng)中取出大量電子密度。這些群體強(qiáng)烈停用群組。另外,由于取代的碳已經(jīng)貧電子,具有諧振貢獻(xiàn)者的任何結(jié)構(gòu),其中有對(duì)碳軸承他吸電子基團(tuán)具有正電荷(即,鄰位或對(duì)位攻擊)比其它的更不穩(wěn)定。因此,這些吸電子基團(tuán)是元導(dǎo)向的,因?yàn)檫@是不具有那么多不穩(wěn)定性的位置。
反應(yīng)也慢得多(相對(duì)于苯的相對(duì)反應(yīng)速率為6×10?-8),因?yàn)榄h(huán)的親核性較低。
對(duì)吡啶的反應(yīng)
與苯相比,由于氮原子的電負(fù)性較高,吡啶上的親電取代速率要慢得多。另外,吡啶中的氮容易通過(guò)質(zhì)子化(來(lái)自硝化或磺化)或用于催化反應(yīng)的路易斯酸(例如AlCl?3)獲得正電荷。這通過(guò)在碳和氮上具有相鄰的形式電荷或在局部原子上具有2個(gè)形式電荷而使反應(yīng)更慢。直接在吡啶中進(jìn)行親電取代幾乎是不可能的。
為了進(jìn)行反應(yīng),它們可以通過(guò)兩種可能的反應(yīng)制備,這兩種反應(yīng)都是間接的。
在吡啶上進(jìn)行取代的一種可能方法是親核芳族取代。即使沒(méi)有催化劑,具有電負(fù)性的氮原子本身也可以保持負(fù)電荷。另一種方法是在親電取代之前進(jìn)行氧化。這使得由氧負(fù)氧原子引起的吡啶N-氧化物使反應(yīng)比吡啶,甚至苯更快。然后氧化物可以還原成取代的吡啶。
Ipso
進(jìn)入基團(tuán)與已經(jīng)帶有取代基(除氫之外)的芳族化合物中的位置的連接。進(jìn)入的基團(tuán)可以取代該取代基,但也可以在隨后的步驟中將其排出或遷移到不同的位置。不使用術(shù)語(yǔ)’?ipso?-substitution’,因?yàn)樗c替換同義。一個(gè)典型的例子是水楊酸與硝酸和硫酸的混合物反應(yīng)形成苦味酸。2位的硝化涉及作為離去基團(tuán)的CO?2的損失。其中磺酰基被質(zhì)子取代的脫磺酸作用是常見(jiàn)的例子。也可以看看林重排。在被硅取代的芳族化合物中,硅通過(guò)取代反應(yīng)而發(fā)生反應(yīng)。
五元雜環(huán)
與苯相比,呋喃,噻吩和吡咯更易受親電子攻擊。這些化合物都含有具有未共用電子對(duì)(氧,硫或氮)的原子作為芳環(huán)的成員,其基本上穩(wěn)定了陽(yáng)離子中間體。吡咯的親電取代的實(shí)例是Pictet-Spengler反應(yīng)和Bischler-Napieralski反應(yīng)。
不對(duì)稱親電芳香取代
通過(guò)轉(zhuǎn)換為手性路易斯酸催化劑,特別是在Friedel-Crafts型反應(yīng)中,用前手性碳親電試劑進(jìn)行的親電芳族取代已經(jīng)適用于不對(duì)稱合成。一個(gè)早期的例子是關(guān)于加入三氯乙醛至酚催化氯化鋁與改性( – ) -薄荷醇。[4]甲乙醛酸化合物已被添加到N,N-二甲基苯胺與手性的二惡唑啉配位體?–?銅(II),三氟甲磺酸催化劑體系也以?Friedel-Crafts羥烷基化:[5]
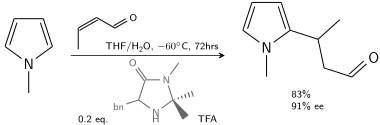
在另一種烷基化中,N-甲基吡咯與用手性咪唑烷酮改性的三氟乙酸催化的巴豆醛反應(yīng):[6]
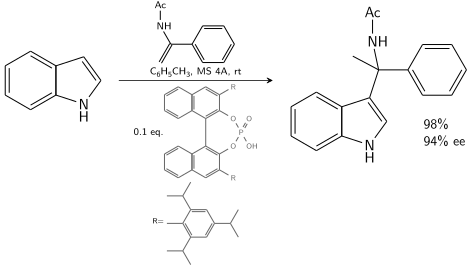
吲哚與手性BINOL衍生的磷酸催化的烯酰胺反應(yīng):[7]
在10-20%手性催化劑存在下,可實(shí)現(xiàn)80-90%ee。
其他反應(yīng)
- 在親電芳族取代模式之后的其他反應(yīng)是一組芳族甲酰化反應(yīng),包括Vilsmeier-Haack反應(yīng),Gattermann Koch反應(yīng)和Reimer-Tiemann反應(yīng)。
- 其他親電子是芳族重氮鹽在重氮偶合,二氧化碳在科爾比-施密特反應(yīng)和活化的羰基在pechmann縮合反應(yīng),hydroxycarbenium離子在布蘭克氯甲基化反應(yīng)通過(guò)中間(羥甲基)芳烴(芐醇),chloryl陽(yáng)離子(CLO?3?+)用于親電子的perchlorylation。
- 在多步驟Lehmstedt-Tanasescu反應(yīng)中,其中一個(gè)親電子試劑是N-亞硝基中間體。
- 在Tscherniac-Einhorn反應(yīng)(以Joseph Tscherniac和Alfred Einhorn命名)中,親電子試劑是酰胺的N-甲醇衍生物